La magia de la luz en la Medicina: la terapia fotodinámica en la lucha contra el Cáncer
Colaboración Especial: Dr. Alfredo Aguilar Elguezabal
Dedicado a la memoria del Dr. Juan Bernal, pionero de esta línea de investigación en nuestro grupo de trabajo, cuyo entusiasmo y dedicación nos inspiraron a seguir avanzando en este fascinante tema.
Sin duda, el empleo de la luz como herramienta en la medicina moderna ha generado alternativas de tratamientos innovadores y no invasivos para diversas afecciones. La Terapia de Luz Roja (Fotobiomodulación) utiliza longitudes de onda específicas de luz roja y cercana al infrarrojo con el fin de estimular procesos celulares, promoviendo la curación y la regeneración de tejidos dañados. Esta técnica se utiliza en el tratamiento de dolores musculares, para atender inflamaciones y como ayuda en la cicatrización de heridas. Otro ejemplo es la Luminoterapia, que consiste en ofrecer a pacientes a la exposición de luz artificial, la cual simula la luz solar.
Esta exposición ayuda en el Trastorno Afectivo Emocional (TAE) y algunos trastornos relacionados con el estado de ánimo. Entre los beneficios están la regulación de ritmos cardiacos y una mejora en la calidad del sueño. Otra tecnología desarrollada es la Terapia con Luz Azul. Este tratamiento se utiliza en dermatología en tratamientos como el acné, ya que además de reducir la inflamación, puede eliminar bacterias que estén presentes en la piel. Todo lo anterior, sin mencionar el uso de láseres para realizar cortes muy precisos y menos invasivos en cirugías, con lo que se reduce el daño a tejidos circundante, lo cual facilita los procesos de recuperación.
Terapia fotodinámica
La terapia fotodinámica (TFD) es un tratamiento médico que combina la aplicación de un agente fotosensibilizador con la exposición a una fuente de luz específica para destruir de una manera selectiva, células anormales, como las cancerosas,. Este enfoque terapéutico ha ganado relevancia en diversas áreas de la medicina debido a su precisión y mínimos efectos secundarios en comparación con tratamientos convencionales.
Los orígenes de la TFD se remontan a principios del siglo XX. En 1905, Von Tappeiner y Jodblauer fueron pioneros en aplicar esta técnica para tratar el cáncer de piel, utilizando eosina (C20H8Br4O5 o C20H8Br2N2O9) como fotosensibilizador y luz blanca como fuente de activación. A lo largo de las décadas, la TFD ha evolucionado significativamente, incorporando nuevos fotosensibilizadores y fuentes de luz más precisas. El porfímero sódico, comercializado como Photofrin, fue el primer fotosensibilizador que obtuvo permiso gubernamental para su uso en TFD clínica, en los años 80´s.
Procedimiento de la Terapia Fotodinámica
Se inicia con la introducción en el organismo de una sustancia fotosensibilizante que se acumula preferentemente en las células anormales, lo cual se logra eligiendo un fotosensibilizador que tenga una elevada afinidad con las células anormales. Esta administración puede ser tópica, aplicando la sustancia directamente sobre la piel, o de otra forma, mediante inyección intravenosa. Después de un período que permite la acumulación del fotosensibilizador en las células objetivo, es decir en donde se localizan las células anormales, se expone la zona afectada a una fuente de luz de longitud de onda específica. Esta luz activa el fotosensibilizador, desencadenando una serie de reacciones que producen especies de radicales que involucran al oxígeno y que son altamente reactivas. De esta manera, las especies activas producen la muerte de las células anormales, preservando las especies sanas del entorno.
Estudio de Azul de Metileno utilizando Nanoliposomas y Nanotubos de Carbono como vehículos en la Terapia Fotodinámica.
Esta investigación forma parte del proyecto denominado «Modulación inducida por láser de la dinámica de membrana celular”, el cual ha sido apoyado por el extinto Fondo Institucional para el Desarrollo Científico, Tecnológico y de Innovación FORDECYT-PRONACES, y se realiza en colaboración entre la Universidad de Guanajuato, CINVESTAV, Unidad Monterrey, CIO, CIATEJ, y CIMAV. Se estudia el uso de nanoliposomas y nanotubos de carbono cargados con azul de metileno para terapia fotodinámica. En particular, se evalúa la capacidad de difusión de estos vehículos cargados con el azul de metileno, hacia el interior de Paramecium tetraurelia, un microorganismo unicelular ciliado de vida libre, que puede ser cultivado en laboratorio. Posteriormente, es decir, una vez que se ha logrado que el vehículo sea llevado al interior del Paramecium, se hace incidir la radiación y se cuantifica el efecto de este tratamiento en la mortandad de los microorganismos.
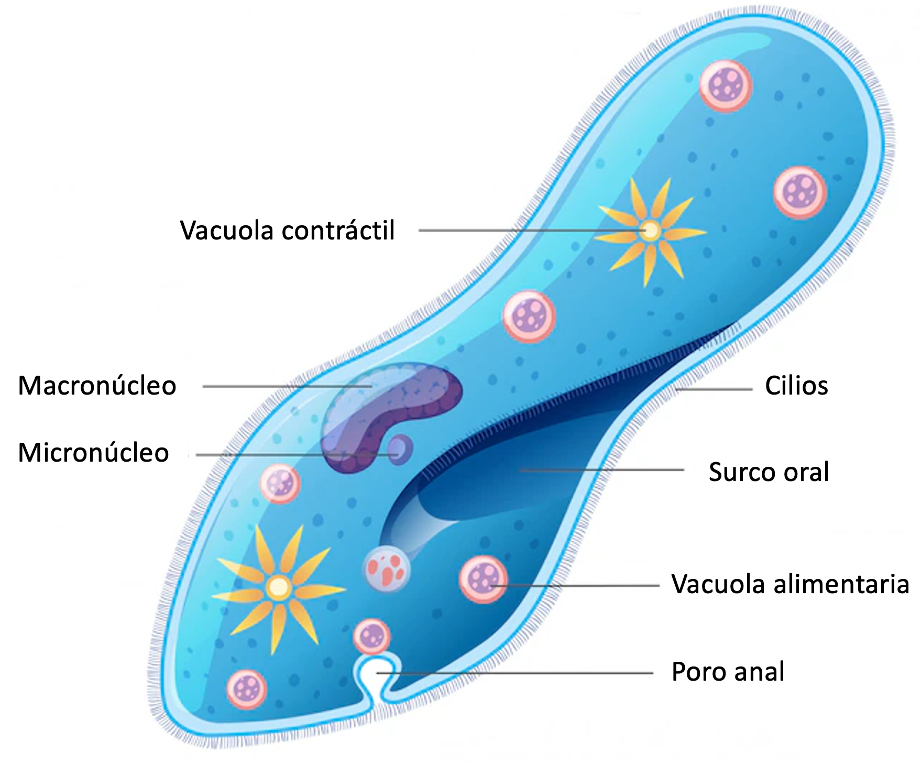
Esquema de la estructura de un Paramecium
Azul de Metileno
Se eligió como fotosensibilizador al azul de metileno, ya que está altamente reportado que al ser irradiado con luz de entre 630 a 680 nm, produce especies reactivas de oxígeno (ROS), las cuales tienen un efecto letal en células, y con el fin de desarrollar estrategias para dirigirlos de manera eficiente hacia las célular a tratar, se estudiaron los dos vehículos seleccionados en este trabajo.
Nanoliposomas
Utilizando lecitina de soya, una molécula que tiene una parte hidrofílica (afín al agua) y una parte hidrofóbica (que repele el agua), y la metodología adecuada, se elaboraron nanoliposomas con un diámetro entre 100 y 200 nanómetros. Estas nanoesferas se componen un una bicapa, que en el exterior tienen la “cabeza” hidrofílica (la parte con mayor polaridad de la molécula), de esta manera al interior tienen la parte no polar (hidrofóbica), pero interactuando con la parte no polar de otra capa interior de lecitina de soya, por lo que la pared interna de la Nanoliposoma queda como la pared externas, con grupos polares expuestos. En esta estructura, al interior del la nanoesfera se concentran las sustancias que actuarán como fotosensibilizador.
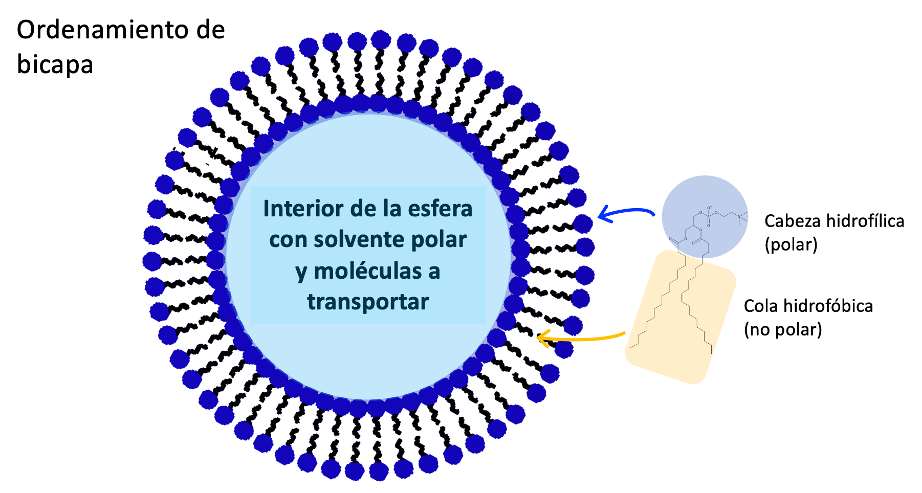
Estructura de las nanoliposomas conformadas en forma de esfera por la bicapa de lecitina, dejando en el interior solvente polar, el cual se utiliza para llevar las sustancias que se quieren transportar al interior de los microorganismos
Nanotubos de Carbono (NTC)
El uso de NTC en este trabajo se debe a que previamente se ha experimentado con los paramecios y su interacción con estos materiales, encontrándose que fácimente traspasan la membrana celular y se difunden en grandes cantidades al interior de éstos, sin que se vean afectados por ello. Adicionalmente, se verificó que el azul de metileno se adsorbe en la superficie de los NTC, siendo un vehículo excelente para su transporte. Los NTC utilizados tienen un diámetro de 52 ± 15 nm y una longitud de 24 ± 9 μm.

Micrografía SEM de Nanotubos de carbono.
La superficie de los nanotubos sirve como medio de transporte del azul de metileno, ya que la moléculas de adsorbe en la pared externa de los nanotubos de carbono.
Experimentación y resultados
La siguiente figura muestra como los NTC previamente impregnado con azul de metileno (AZ) tras 5 minutos de contacto con los paramecium puestos en un portaobjetos, ingresan al interior de del microorganismo.

Figura 3. Micrografía de Paramecium tetraurelia, previo a administrar nanotubos de carbono, no se observan estructuras oscuras en su interior (A). Paramecium tetraurelia con nanotubos de carbono en su interior, imagen obtenida 5 minutos después de la administración de estos (B).
Los experimentos con Paramecium se llevaron a cabo en microplacas de 96 pozos de fondo plano. Se concentraron los medios con Paramecium, centrifugándolos y decantando el medio. En cada pozo de la microplaca se depositaron 10 μl de Paramecium concentrado, se realizó un conteo inicial para obtener la población inicial y se aplicaron los distintos tratamientos, y al término del tratamiento se dio un tiempo de 5 minutos, para posteriormente realizar el conteo final de células. Se hicieron 5 réplicas de cada tratamiento realizado.
Las pruebas estadísticas realizadas mostraron que si existe un decremento de población significativo en los ensayos fotodinámicos. Y de igual forma mostraron que la aplicación de los materiales y los láseres por sí solos no produce decrementos significativos de la población, así que la efectividad es el resultado de un efecto sinérgico de los materiales y la incidencia de radiación láser de 650 nm.
Los resultados muestran una alta eficacia de la terapia fotodinámica con ambos nanomateriales, superando el 90% de mortalidad en Paramecium. Las pruebas de terapia fotodinámica muestran que un tiempo de exposición de 5 minutos a la luz de 650 nm, es suficiente para llevar el efecto fotodinámico y producir muerte celular.
Este trabajo utilizó un modelo biológico simple, de fácil acceso, su reproducción relativamente sencilla y barata, y su manejo sin necesidad de equipo especializado. Es importante considerar los resultados obtenidos para su uso en líneas celulares
Estos resultados sugieren que las nanoliposomas y nanotubos de carbono cargados con azul de metileno son candidatos prometedores para el desarrollo de nuevas terapias fotodinámicas para el tratamiento de diversas enfermedades. La combinación de la TFD con la actividad fototérmica de los nanotubos de carbono abre nuevas posibilidades para el tratamiento de enfermedades, especialmente en el campo del cáncer.
Sin embargo, es importante destacar que se requiere de mayor investigación para evaluar la seguridad y eficacia de estos nanomateriales en modelos biológicos más complejos y en ensayos clínicos. La experimentación de este trabajo ha sido realizada por Carlos Alberto Aranda Sánchez como parte de formación en la Maestría en Ciencia de Materiales, bajo la Dirección de los Dres. Alfredo Aguilar y Natanael B. Cuando, y el apoyo del equipo técnico del Laboratorio de Nanopartículas, Dr. Manuel Román.
Referencias
S. Kwiatkowski et al., “Photodynamic therapy – mechanisms, photosensitizers and combinations,” Biomedicine and Pharmacotherapy, vol. 106. Elsevier Masson SAS, pp. 1098–1107, Oct. 01, 2018. doi: 10.1016/j.biopha.2018.07.049.
Y.-D. Lee et al., “Topical methylene blue nanoformulation for the photodynamic therapy of acne vulgaris,” Arch Dermatol Res, vol. 315, no. 4, pp. 885–893, Nov. 2022, doi: 10.1007/s00403-022-02464-7.
J. Hao et al., “Encapsulation of the flavonoid quercetin with chitosan-coated nano-liposomes,” LWT – Food Science and Technology, vol. 85, pp. 37–44, Nov. 2017, doi: 10.1016/j.lwt.2017.06.048.
A. Aguilar-Elguézabal, W. Antúnez, G. Alonso, F. P. Delgado, F. Espinosa, and M. Miki-Yoshida, “Study of carbon nanotubes synthesis by spray pyrolysis and model of growth,” Diam Relat Mater, vol. 15, no. 9, pp. 1329–1335, Sep. 2006, doi: 10.1016/j.diamond.2005.10.011.


